(Solved): Question 4 (8 pts) Vous voulez tudier la cintique chimique de la raction hypothtique suivan ...
Question 4 (8 pts) Vous voulez étudier la cinétique chimique de la réaction hypothétique suivante:
2A+B+C->2DEn utilisant les données du tableau suivant déterminées pour cette réaction à
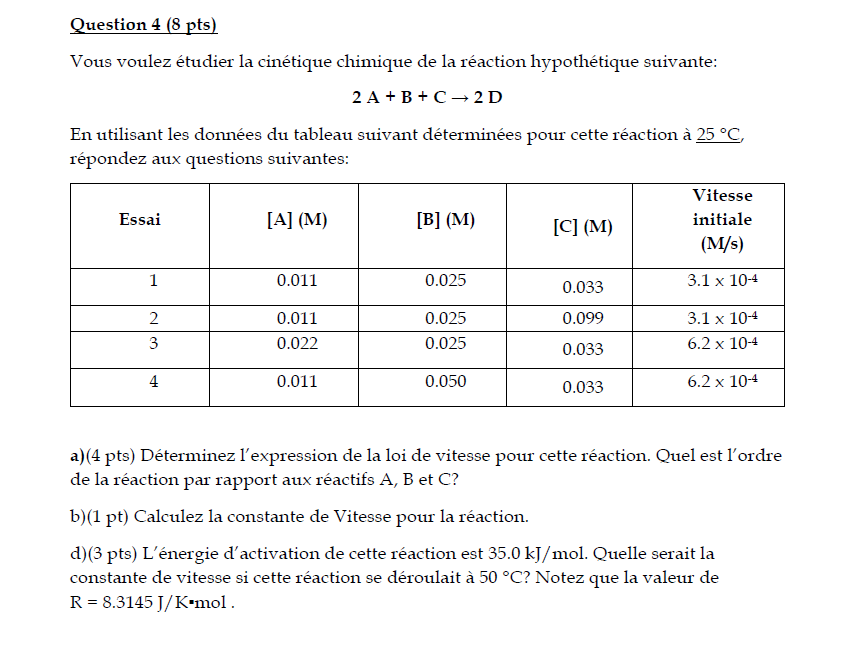
25\deg C, répondez aux questions suivantes: \table[[Essai,[A] (M) (M),\table[[Vitesse],[initiale],[[M/s)]],,],[1,0.011,0.025,0.033,3.1\times 10^(-4)],[2,0.011,0.025,0.099,3.1\times 10^(-4)],[3,0.022,0.025,0.033,6.2\times 10^(-4)],[4,0.011,0.050,0.033,6.2\times 10^(-4)]] a)(4 pts) Déterminez l'expression de la loi de vitesse pour cette réaction. Quel est l'ordre de la réaction par rapport aux réactifs
A,Bet C ? b)(1 pt) Calculez la constante de Vitesse pour la réaction. d)(3 pts) L'énergie d'activation de cette réaction est
35.0k(J)/(m)ol. Quelle serait la constante de vitesse si cette réaction se déroulait à
50\deg C? Notez que la valeur de
R=8.3145(J)/(K)*mol.